روش اندازهگیری سختی، کلسیم و منیزیم در آب
- روش اندازهگیری سختی، کلسیم و منیزیم در آب
- سختی HARDNESS
- انواع سختی
- 1- سختی کل (TOTAL HARDNESS) :
- 2- سختی کلسیم و منیزیم :
- 3- سختی موقت یا کربنات:
- 4- سختی دائم یا سختی غیرکربنات:
- 5- سختی کاذب:
- روشهای تعیین سختی آبها
- مزاحمتها و نحوه حذف آنها:
- مواد و محلولهای مورد نیاز:
- پوشاننده شماره 2:
- پوشاننده شماره 3:
- 2- شناساگر اریوکرم بلاک (T) تی:
- 3- محلول تامپون:
- 4- محلول EDTA:
- 5- محلول 50 گرم بر لیتر سود سوزآور
- 6- کلریدریک اسید یک نرمال
- روش آزمایش:
- روش اندازهگیری کلسیم
- روش اندازهگیری منیزیم
روش اندازهگیری سختی، کلسیم و منیزیم در آب
سختی HARDNESS
کاتیون فلزات دو ظرفیتی عامل اصلی سختی آبها میباشند. مهمترین کاتیونهای ایجاد کننده سختی در آب عبارتند از: کلسیم، منیزیم، استرانسیوم، آهن دو ظرفیتی و منگنز، نظر به اینکه استرانسیوم، آهن و منگنز در آبهای صنعتی به مقدار جزئی وجود دارند. بنابراین میتوان کلسیم و منیزیم را به عنوان عامل اصلی ایجاد سختی در آب نام برد. جدول زیر (جدول 1) مهمترین کاتیونهای ایجاد کننده سختی و آنیونهای وابسته به آنها را نشان میدهد. آلومینیوم و آهن سه ظرفیتی بعضی مواقع به سختی آب کمک میکنند.
ولی حلالیت آنها در آبهای طبیعی به اندازهای محدود میباشد که میتوان از غلظتهای آنها صرف نظر نمود.
جدول 1- مهمترین کاتیونهای ایجاد کننده سختی و آنیونهای وابسته به آنها

انواع سختی
1- سختی کل (TOTAL HARDNESS) :
مربوط به املاح کلسیم و منیزیم میباشد شامل از کلرور، سولفات، کربنات و…
2- سختی کلسیم و منیزیم :
ممکن است تعیین سختی کلسیم و سختی منیزیم به طور جداگانه لازم باشد، در صورتی که نیاز به مقادیر جداگانه داشته باشد مطابق زیر عمل نمایید.
سختی منیزیم + سختی کلسیم = سختی کل
سختی کل – سختی کلسیم = سختی منیزیم
3- سختی موقت یا کربنات:
این نوع سختی به کربنات و بیکربناتهای کلسیم و منیزیم مربوط میباشد که در اثر بالارفتن درجه حرارت رسوب میکند، ( این عمل با نیمساعت جوشاندن انجام میشود) 100 میلیلیتر نمونه را بجوشانید سپس صاف نمایید و توسط آب بییون به حجم برسانید ( جهت سختی دائم)
4- سختی دائم یا سختی غیرکربنات:
این سختی مربوط به کلرورها، سولفاتها، نیتراتهای کلسیم و منیزیم میباشد و از این جهت سختی دائم گویند چون در اثر جوشاندن ایجاد رسوب و گازکربنیک نمیکند.
سختی کل – سختی کربنات = ( سختی غیر کربنات) سختی دائم
5- سختی کاذب:
وقتی مقدار زیادی سدیم در آب وجود داشته باشد ایجاد سختی کاذب مینماید.
روشهای تعیین سختی آبها
1- روش محاسبه:
شاید دقیقترین روش تعیین سختی آبها روش محاسبه میباشد که از طریق تعیین یونهای دو ظرفیتی ایجاد کننده سختی در آب مشخص میگردد. محاسبه از طریق فرمول زیر صورت میگیرد.
M++(mg/Lit)×50/ME++ PPm =سختی بر حسب کلسیم کربنات
++ ME =عدد اکیوالان یون مورد نظر
50 = عدد اکیوالان کلسیم کربنات
مثال: تعیین کنید سختی نمونه آبی را که نتایج آنالیز آب به شرح زیر میباشد.

با توجه به این که فقط کاتیونهای دو ظرفیتی +Ca2+، Mg2+، Sr2 عامل ایجاد کننده سختی میباشند.

به طور کلی با داشتن مقدار یونهای ایجاد کننده سختی و استفاده از فرمول زیر میتوان سختی کل را محاسبه نمود.
( مقدار کلسیم بر حسب 2/5×Ca+2) = سختی کل بر حسب کلسیم کربنات … + … + (مقدار منیزیم بر حسب 4/12×Mg+2 ) +
2- روش تیتراسیون:
اساس روش فوق بر پایه تشکیل دو کمپلکس مختلف با ثابت تشکیلهای متفاوت از اریوکرم بلاکتی و EDTA میباشد. ابتدا با اضافه کردن محلول اریوکرم بالاکتی 10= pH –کمپلکس قرمز رنگی با یونهای ایجاد کننده سختی به وجود میآید. سپس با اضافه نمودن EDTA کمپلکس فلزی- اریوکروم بالاکتی جای خود را به کمپلکس فلزی -EDTA آبیرنگ میدهد. این عمل به این دلیل اتفاق میافتد که ثابت تشکیل کمپلکس اول 1/10 ثابت تشکیل کمپلکس دوم میباشد. تغییر در این نسبت موجب ایجاد نقطه پایانی زودرس یا دیررس خواهد شد.

مزاحمتها و نحوه حذف آنها:
در اندازهگیری سختی، رنگ، مواد معلق و مواد کلوئیدی آلی ایجاد مزاحمت مینمایند همچنین اکثر یونهای فلزی در این آزمایش مزاحم هستند، زیرا آنها نیز با EDTA تیتر میشوند و همچنین میتوانند نقطه ختم عمل را بپوشانند. این مزاحمتها را میتوان توسط مواد شیمیایی (INHIBITOR) قبل از تیتر کردن EDTA رسوب داد و یا به صورت انواع یونهای کمپلکس در آورد. جدول زیر (جدول 2) ماکزیمم مقادیر قابل قبول مزاحمها را در نمونه در صورتی که از inhibitor استفاده نمایید نشان میدهد. در مکانهایی که ستاره وجود دارد نشان میدهد که حتی در حضور inhibitor یا پوشاننده این اجسام با EDTA تیتر میشوند و در سختی اثر میگذارند.
جدول 2- ماکزیمم مقادیر قابل قبول مزاحمها

مواد و محلولهای مورد نیاز:
پوشاننده شماره 1- KCN :
پتاسیم سیانید، این پوشاننده به صورت پودر و به مقدار 0/25 گرم جهت هر آنالیز استفاده میشود. دقت کنید پتاسیم سیانید به شدت سمی است. از هرگونه تماس خودداری شود.
پوشاننده شماره 2:
5 گرم سدیم سولفید Na2S,9H2O یا 3/7 گرم Na2S,5H2O را در 100 میلیلیتر آبمقطر حل نمایید و در شیشه کدر نگهداری نمایید. با توجه به سریع اکسید شدن، محلول را دور از هوا قرار دهید و برای آزمایش یک میلیلیتر آن را استفاده نمایید. چون معرف در شرایط قلیایی بیثبات میباشد عمل تیتراسیون را باید سریع انجام دهید.
پوشاننده شماره 3:
4/5 گرم از هیدروکسیل آمینهیدروکلرید را در 100 میلیلیتر اتیلیک الکل 95 درصد حل نمایید (یا ایزوپروپیل الکل).
2- شناساگر اریوکرم بلاک (T) تی:
0/5 گرم از این شناساگر را با 100 گرم نمک طعام بسابید و خشک کنید ( در دمای C° 100 به مدت 24 ساعت) و به خوبی مخلوط نمایید و در صورت لزوم ساییده و دور از رطوبت نگهداری کنید.
3- محلول تامپون:
16/9 گرم آمونیوم کلرید را در 143 میلیلیتر آمونیاک غلیظ حل نمایید و حجم آن را با آبمقطر به 500 میلیلیتر برسانید.
4- محلول EDTA:
(نمک سدیمی، اتیلن دیآمین، تترااستیک اسید) نمک مورد استفاده باید قبل از وزن شدن به مدت 5 ساعت در C° 80 خشک کنید. 37/224 گرم از نمک را با دقت وزن کنید و با آب بدون یون به حجم یک لیتر برسانید ( محلول حاصل M 0/1 میباشد).
میلیگرم کلسیم 4/008 = یک میلیلیتر محلول بالا
5- محلول 50 گرم بر لیتر سود سوزآور
6- کلریدریک اسید یک نرمال
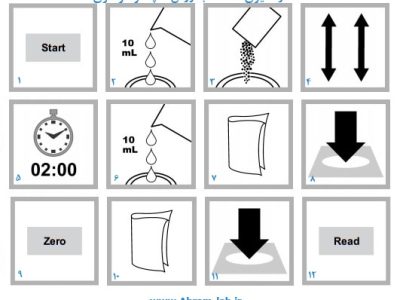
روش آزمایش:
به 100 میلیلیتر نمونه 5 میلیلیتر ( یا مقادیر بیشتر جهت تنظیم 10= Ph) اضافه نمایید سپس با نوک کاردک از شناساگر اریوکرم بلاکتی اضافه کنید و در حالی که مرتب محلول را به هم بزنید با محلول M 0/1 EDTA ( نمک سدیم آن) تا ایجاد شدن رنگ آبی تیتر نمایید. در صورتی که محلولهای پوشاننده نیاز باشند پس از برداشتن نمونه آن را اضافه نمایید. با استفاده از رابطه مذکور مقدار سختی را بر حسب کلسیم کربنات به دست آورید.
سختی کل (میلیگرم بر لیتر) = a×10×1000/V
a= میلیلیتر مصرفی M 0/1 EDTA
V= حجم نمونه مورد آزمایش
روش اندازهگیری کلسیم
میتوان جهت اندازهگیری کلسیم از روشهای مختلف استفاده کرد. روشهای حجمی ماده تیتر کننده محلول نمک سدیم EDTA میباشد ولی میتوان جهت تعیین پایان واکنش از شناساگرهایی مانند موراکسید، کالکن کربوکسیلیک اسید استفاده نمود.
اندازهگیری کلسیم با استفاده از شناساگر (MUREXIDE) به روش تیتراسیون
در اندازهگیری کلسیم، مزاحمتهای مختلفی از طرف فلزات میتواند وجود داشته باشد که جهت پوشش آنها مطابق زیر عمل نمایید.
مزاحمتهای منیزیم را با افزودن هیدروکسید قوی از بین ببرید، اثر منگنز توسط هیدروکسیل آمین با سولفات هیدرازین برطرف میشود، مزاحمت مس و روی توسط سدیم سولفید از میان میرود و اثرات کادمیم، کبالت، نیکل، جیوه و به طور کلی فلزات سنگین را میتوان با سدیم سولفید و یا پتاسیم سیانید حذف نمایید.
روش آزمایش:
به 100 میلیلیتر نمونه خنثی برای رسیدن به pH= 12 ، دو (2) میلیلیتر محلول سود سوزآور اضافه نمایید آنگاه توسط کاردک مقدار مورکسید به محلول اضافه کنید و در حال بهم زدن با محلول تیتر کننده EDTA ( نمک سدیم اتیلن دی آمین تترااستیک اسید) تیتر نمایید تا تغییر رنگ حاصل شود. در این آزمایش میتوان از شناساگر کالکن کربوکسیلیک اسید استفاده نمایید که تغییر رنگی آن از قرمز به آبی واضحتر باشد. با استفاده از رابطه زیر مقدار کلسیم را محاسبه نمایید.
(Ca++)میلیگرم بر لیتر = a×4/008×1000/V
روش اندازهگیری منیزیم
به دو طریق میتوان مقدار منیزیم را محاسبه نمود:
اولین راه این است که با در دست داشتن سختی کل و سختی کلسیم و استفاده از فرمول زیر مقدار منیزیم را محاسبه نمایید.
سختی کل – سختی کلسیم = سختی منیزیم
در روش دوم: محلول حاصل از اندازهگیری کلسیم را توسط کلریدریک اسید یک نرمال خنثی نمایید و سپس عملیاتی که جهت آزمایش سختی انجام میدادید روی این نمونه نیز انجام دهید و با کمک رابطه زیر مقدار منیزیم را محاسبه نمایید.
a×2/43×1000/V = میلیگرم بر لیتر منیزیم
a= میلیلیتر مصرفی ماده تیتر کننده
V= حجم نمونه مورد آزمایش
یک میلیلیتر محلول M 0/1 ماده تیترکننده برابر 2/431 میلیگرم Mg2+ و 4/031 میلیگرم MgO میباشد.
مواد و محلولهای مورد نیاز:
1- شناساگر موراکسید murexide
0/2 گرم از این معرف را با 100 گرم نمک طعام ( که قبلاً در C° 100 خشک گردیده) در هاون بسابید و در جای مناسب دور از رطوبت نگهداری کنید.
2- کلریدریک اسید یک نرمال
3- محلول سود سوزآور یک نرمال یا بیشتر جهت تنظیم pH
لازم به یادآوری میباشد که میتوان شناساگرها را توسط الکل به صورت مایع در آورد.