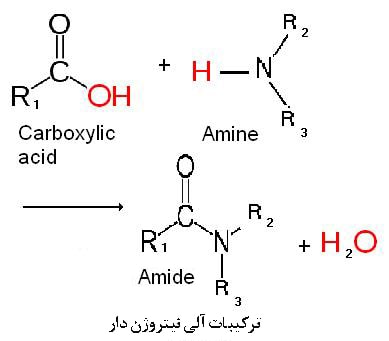
ترکیبات آلی نیتروژن دار
ترکیبات آلی نیتروژن دار
از نظر شیمی تجزیه، نیتروژن آلی به نیتروژن مقید در مواد آلی با حالت اکسایش 3- گفته می شود؛ به طوری که بتوان آن را با روش کِلدال اندازه گیری کرد. در روش کِلدال، نیتروژن تمام ترکیبات آلی نیتروژن دار اندازه گیری نمی شود؛ بلکه نیتروژن مواد آلی طبیعی همچون پروتئین ها، پپتیدها، نوکلوئیک اسیدها و اوره و نیز نیتروژن بسیاری از ترکیبات آلی سنتزی اندازه گیری می شود و این روش نمی تواند نیتروژن ترکیبات آلی همچون آزید، ترکیبات آزو، نیتریل، ترکیبات نیترو، ترکیبات نیتروزو و هیدرازین را اندازه گیری کند. در روش کِلدال، نیتروژن آمونیاکی که دارای حالت اکسایش 3- است نیز همراه با نیتروژن آلی اندازه گیری می شود؛ به طوری که کل نیتروژن کِلدال (TKN)، مجموع نیتروژن آلی و کل نیتروژن آمونیاکی است.
در روش کلدال، نمونه آب به کمک اسید و حرارت، هضم شده تا نیتروزن آلی آن به آمونیوم تبدیل شود. سپس نیتروژن آمونیاکی تولیدشده اندازه گیری می شود. در صورتی که فقط اندازه گیری نیتروژن آلی آب (بدون نیتروژن آمونیاکی) موردِ نظر باشد، باید قبل از هضم، نمونه را جوشانده تا تمام آمونیاک آن از محلول خارج شود. در ضمن، از تفریق مقادیر کل نیتروزن کِلدال و کل نیتروژن آمونیاکی نیز می توان نیتروزن آلی را برآورد کرد.
از روش های اکسایش نورشیمیایی نیز می توان به جای روش کلدال برای اندازه گیری نیتروژن آلی استفاده کرد. در این روش ها، نیتروژن آلی و نیتروژن آمونیاکی به نیترات اکسیده و سپس مقدار آن اندازه گیری می شود. البته قبل از اکسایش نورشیمیایی، باید مقادیر نیترات و نیتریت زمینه موجود در نمونه را اندازه گیری کرد. اگر نمونه، قبل از آزمایش کِلدال یا نورشیمیایی از صافی عبور کند، آنگاه نیتروژن آلی محلول (به جای کل نیتروژن آلی) تعیین مقدار می شود.
غلظت های نیتروژن آلی آب های طبیعی از چند میکروگرم بر لیتر در آب بعضی از دریاچه های تمیز بیش از20 mg N/Lدر فاضلاب خام متغیر است. در استانداردهای آب آشامیدنی، معمولاً حد مجازی برای نیتروژن آلی تعیین نشده است، ولی بعضی از آنها (مثل استاندارد EU) حد مجازی برای کل نیتروژن کلدال مشخص کرده اند. در استاندارد EU، حداکثر مجاز نیتروژن کلدال mg N/L 1 مقرر شده است.
ترکیبات آلی نیتروژن دار به فرم های متفاوتی مانند آزاید ، آزین ، آزو ، هیدازون ،نیترات ، نیتریت ، نیترایل ، نیترو ، نیتروسو، اکسیمو، سمی – کربوزون در آب یافت می شود. نیتروژن آلی برابر است با جمع نیتروژن آلی و نیتروژن آمونیاکی. عامل اصلی که در انتخاب یک روش ماکرو یا نیمه میکرو کجلدال تأثیر می گذارد ، تعیین نیتروژن آلی و غلظت آن است. روش ماکرو کجلدال برای نمونه های قابل استفاده است که در نمونه ها که حاوی غلظت کم یا زیاد نیتروژن آلی هستند، اما نسبتا حجم نمونه بزرگ برای غلظت های پایین مورد نیاز است.
در روش نیمه میکرو کجلدال ، که برای نمونه های حاوی غلظت بالای نیتروژن آلی است. حجم نمونه باید شامل مواد آلی به علاوه نیتروژن آمونیاکی در محدوده 0.2 تا 2 میلی گرم باشد. روش هضم نمونه (D)، یک روش میکرو با یک مرحله تجزیه و تحلیل خودکار قادر اندازه گیری نیتروژن آلی به میزان 0.1 میلی گرم در لیتر است هنگامی که نمونه های شاهد با دقت کنترل شوند.
همیشه قابل اطمینان ترین نتایج در نمونه های تازه بدست می آید. اگر یک آنالیز فوری نباشد، می توان نمونه هایی برای هضم کجلدال را با اسیدی که میزان پی اچ آن 1.5 تا 2.0 است با غلظت اسید سولفوریک و در دمای 4 درجه سانتیگراد نگه داری کرد.
مزاحمت در اندازه گیری ترکیبات آلی نیتروژن دار
در طول هضم نمونه برای هضم کجلدال، اگر مقدار نیترات نمونه بیشتر از 10 میلی گرم در لیتر باشد ، می تواند بخشی از آمونیاکی که از نیتروژن آلی قابل هضم تولید می شود را اکسید کند که درنتیجه باعث تولید N2O و ایجاد تداخل منفی در نتیاج می شود. هنگامی که مواد آلی کافی در حالت اکسیداسیون کم وجود دارد، نیترات را می توان به آمونیاک کاهش داد و منجر به مزاحمت مثبت شد.
شرایط که تحت تداخل های قابل توجهی رخ می دهد به خوبی تعریف نشده است و هیچ راه اثبات شده ای وجود ندارد تا مزاحمت را در ارتباط با روش های کجلدال که در اینجا شرح داده شد را از بین ببرد.
محتوای اسید و نمک که از واکنش هضم کجلدال تولید می شود برای تولید دمای هضم در حدود 380 درجه سانتی گراد است. اگر نمونه دارای مقادیر بسیار بزرگی نمک یا مواد جامد معدنی باشد که در طول هضم ایجاد شده است، درجه حرارت بالا می تواند تا 400 درجه سانتیگراد افزایش یابد، که در آن نقطه از دست دادن نیتروژن خورشیدی آغاز می شود. برای جلوگیری بیش از حد دمای هضم، باید مقادیری H2SO4 اضافه کرد تا حفظ تعادل اسید و نمک انجام بگیرد. همه نمکها باعث افزایشدما افزایش به یک اندازه نمی شوند. اما اضافه کردن 1 میلی لیتر بر گرم H2SO4 نمک در نمونه باعث نتایج معقولی می شود.
اضافه کردن اسید و ایجاد واکنش هضم در هر دو نمونه و شاهد اضافه شود. اسید بیش از حد ، دمای هضم را در زیر 380 درجه سانتیگراد پایین می آورد و موجب هضم و بازیابی ناتمام می شود. در صورت لزوم، قبل از نهایی شدن فرآیند مقدار سدیم هیدروکسید سدیم تیوسولفات را به نمونه اضافه کنید.










