روش اندازهگیری سولفات در آب
روش اندازهگیری سولفات در آب
از روشهای اندازه گیری سولفات در آب ما دو روش اندازهگیری نورسنجی و روش تیتراسیون را در اینجا توضیح میدهیم. سولفات یکی از تستهای شیمیایی آب میباشد که در شرکت دانش بنیان آب راهبر محاسب (آبرام) آزمایش میشود. علاوه بر این تست، تستهای دیگر شیمیایی، میکروبی، فلزات سنگین و غیره در این آزمایشگاه آزمایش میشود. جهت ارسال نمونه آب جهت آزمایش با کارشناس تماس بگیرید.

روش نورسنجی
روشی که در زیر خواهد آمد روش نورسنجی اندازهگیری مقدار سولفات میباشد، در این روش سولفات بر حسب ppm اندازهگیری میشود. یون سولفات با نمکهای باریم، رسوب باریم سولفات ایجاد مینمایید. با توجه به شرایط به کار برده شده در آزمایش، رسوب تولید شده به صورت سوسپانسه در داخل محلول یکنواخت است و تولید کدری مینماید که شدت کدری بسته به غلظت یون سولفات در نمونه دارد.
– حساسیت این آزمایش ppm1 و کمترین مقدار اندازهگیری ppm2 و ماکزیمم ppm20 میباشد.
مواد و محلولهای مورد نیاز:
1- محلول استاندارد سولفات: 1/375 گرم از نمک آمونیوم سولفات (NH4)2SO4 را در یک لیتر آب حل نمایید. 1=1mgSO4 میلی لیتر
2- محلول اسیدی نمک طعام: 240 گرم نمک طعام را در آب حل نمایید و به آن 20 میلیلیتر کلریدریک اسید Conce اضافه نمایید. سپس محلول را به حجم یک لیتر برسانید.
3- محلول رقیق گلیسیرین 50 درصد حجمی
4- کریستال باریم کلرید (BaCl2 ,2H2O)
روش آزمایش:
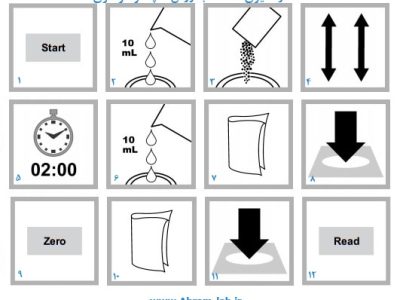
به 100 میلیلیتر نمونه 10 میلیلیتر اسیدی نمک طعام اضافه نمایید، آنگاه 10 میلیلیتر گلیسیرین و 0/2 گرم باریم کلرید اضافه کنید و به مدت یک دقیقه به هم بزنید و 10 دقیقه نمونه را کنار بگذارید و سپس به هم بزنید و جذب را روی طول موج nm440 یا nm425 اندازهگیری نمایید و با استفاده از منحنی استاندارد مقدار سولفات را مشخص نمایید. جهت شاهد از آب مقطر و معرفهای ذکر شده فوق استفاده نمایید.
روش تیتراسیون
روش 1: در این روش ابتدا نمونه را از روی یک فیلتر کاتیونی قوی عبور دهید تا اسیدهای مربوطه حاصل شود آنگاه با اضافه کردن باریم کلرید و رسوب دادن سولفات به صورت باریم سولفات و اندازهگیری باریم باقیمانده در حضور یون منیزیم به روش تیتراسیون با EDTA مقدار سولفات را مشخص نمایید.
مواد و محلولهای مورد نیاز:
1- رزین کاتیونی قوی که با کلریدریک اسید شستوشو داده شده باشد.
2- محلول M 0/01 باریم کلرید: جهت تهیه این محلول مقدار مشخصی از نمک آن را وزن کنید و به حجم یک لیتر برسانید. 1=0/96mgSO4— میلیلیتر محلول
3- محلول 0/01 M از منیزیم یا ترکیبات منیزیم 1=1mgCaCO3 میلی لیتر محلول
4- محلول M 0/01 از نمک EDTA ( طرز تهیه در آزمایش سختی آورده شده است)
5- محلول بافر ( طرز تهیه در آزمایش سختی آورده شده است)
روش آزمایش:
600-500 میلیلیتر نمونه را از روی فیلتر کاتیونی با سرعت lit/min 0/4- 0/3 عبور دهید و 300-200 میلیلیتر نمونه اولیه را دور بریزید و 100 میلیلیتر آن را در ظرف مناسب بجوشانید و در همان حال قطره قطره 15 میلیلیتر باریم کلرید به آن اضافه نمایید به مدت 15 دقیقه آن را به هم بزنید با گرم کردن 10 میلیلیتر محلول 0/01 مولار منیزیم کلرید و 5 میلیلیتر بافر، (10-8) قطره E.B.T اریوکرم بلاکتی اضافه نمایید و با محلول EDTA یا نمک آن تیتر نمایید تا رنگ محلول از قرمز به آبی برگردد. بر روی یک نمونه آب مقطر عاری از سولفات نیز عملیات فوق را انجام دهید. مقدار سولفات را از رابطه زیر به دست آورید.