وزن سنجی یا گراویمتری
وزن سنجی یا گراویمتری
وزن سنجی یا گراویمتری (گراویمتری در شیمی تجزیه ) عبارت است از اندازه گیري کمی یـک جسـم از طریـق رسـوب دادن آن و جـدا کـردن و توزین رسوب حاصل . به این صورت عمل می شود که وزن معینی از نمونـه شـامل جسـم مجهـول در حلال مناسبی حل می شود. سپس محلول رسوب دهنده به مقدار زیاد اضافه می گردد. رسوب حاصل پس از صاف کردن، شستن خشک کردن و افروزش توزین می گردد. با توجه به وزن و ترکیب رسـوب حاصل مقدار یونهاي رسوب کرده و با در نظـر گـرفتن وزن نمونـه درصـد جسـم مجهـول در نمونه محاسبه می گردد. روش وزن سنجی چون بر اساس توزین است داراي صحت و دقت( حدود 0.1 %) زیاد می باشد ولی عیب آن این است که وقت زیاد می گیرد. در زیر گراویمتری برای اندازه گیری سولفات تشریح می گردد.
وزن سنجی یا گراویمتری سولفات
سولفات باریم با داشتن ثابت انحلال خیلی کم بهترین رسوب در تعیین مقدار سولفات است. بعلاوه این جسم در نتیجه حرارت زیاد ، تغییری نکرده و ثابت باقی می ماند. ذرات سولفات باریم تشکیل شده معمولا ریز بوده و ممکن است از جدار کاغذ صافی عبور نماید بـراي حل این مشکل بهتر است هنگام اضافه نمودن نمک باریم عمل را به آهستگی تمام انجام داد.
محلولهاي مورد نیاز :
- هیدرو کلریدریک اسید 2مولار
- باریم کلرید %3وزنی – حجمی
- نیتریک اسید 2مولار، نیترات نقره جهت تست کلر
شرح آزمایش وزن سنجی یا گراویمتری سولفات :
- مجهول داده شده اگر به صورت جامد می باشد توسط قیف بـه بـالن ژوژه منتقـل و پـس از حـل کردن با آب مقطر به حجم برسانید و اگر محلول می باشد مسـتقیما توسـط آب مقطـر بـه حجـم برسانید.
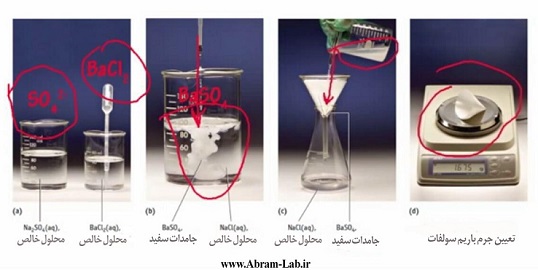
- یک بشر برداشته و 25میلی لیتر از محلول سولفات داده شده را در بشر بریزید. بشر ۲۵
- 3تا 5میلی لیتر HCl دو مولار به محلول افزوده سپس آنرا حرارت دهید (تا نزدیک جوش)
- توسط پیپت مدرج و یا بورت قطره قطره محلول کلرید باریم %3به محلول اضافه کرده و دائما بـا همزن شیشه اي آنرا به هم بزنید (توجه داشته باشید که همزن به جدار و ته بشر سـائیده نشـود) افزایش باریم کلرید را ادامه دهید تا رسوب سولفات باریم کامل شود. سپس درب ظرف را با کاغـذ بسته و صبر کنید تا عمل رسوب گیري کامل شود.
- یک کروزه تمیز را به مدت یک ربع ساعت در حرارت 700-800درجه سانتیگراد در کوره قـرار داده و سپس در دسیکاتور قرار دهید تا خنک شود. وزن دقیق آنرا تعیین کنید.
- بعد از آنکه رسوب ها ته نشین شد به کمک کاغذ صافی باند آبی آنرا صاف کنید. ابتدا بدون هم زدن محلول روئی بشر را از کاغذ صافی عبور دهید. آنقدر این عمل را تکرار کنید تا محلول زیـر صافی شفاف باشد.
- به کمک شستشو با آب مقطر گرم که آن را داخل بشر ریخته و هم زده اید یونهاي کلر موجود در رسوب را از آن خارج کرده و در ضمن رسوب ها را روي کاغذ صافی انتقال دهید.
- راي اطمینان از نبودن کلر تست نیترات نقره را انجام دهید. براي این کار حدود یک میلی لیتر از آخرین محلول زیر صافی را وارد لوله آزمایش کرده و یک قطره نیتریـک اسـید 1مـولار و چند قطره نقره نیترات %1به آن اضافه کنید. در صورتی که کدر شد دلیل بـر وجـود کلـر در محلول زیر صافی است.
- پس از خاتمه صاف کردن کاغذ صافی، محتوي رسوب را جمع کرده در کـروزه کـه وزن آنـرا بـه دست آورده اید قرار دهید به کمک چراغ گاز با شعله کم آنرا حرارت داده تا ابتدا خشک و سپس با زیاد کردن شعله بسوزد و خاکستر شود. کروزه محتـوي رسـوب را در کـوره 700-800درجـه سانتی گراد به مدت 20دقیقه قرار داده پس از خاتمه زمان لازم آنرا در دسیکاتور گذاشته تـا پس از سرد شدن وزن کنید و غلظت سولفات را بدست آورید.










چرا از hcl استفاده میکنیم
ببخشید متوجه منظور شما نشدم.
سلام
ممنون از مطلب مفیدتون
ماده ای به نام ائوزین یلو را چطور میتوان تیتراسیون گراویمتری کرد؟
سلام ممنون… در این زمینه اطلاعی ندارم متاسفانه
چرا در این واکنش از هیدروکلریک اسید استفاده می کنیم
سلام در دستور کار ذکر شده و به خاطر اسیدی کردن محیط اضافه می شود.
سلام چرا موقع رسوب گیری باید محلول هم زده بشه ؟ و علت گذاشتن رسوب در حمام برای چیه ؟
سلام وقتتون بخیر
تا رسوب گیری به صورت کامل انجام شود.
برخی کاتیونهای فلزی در محیط قلیایی به صورت هیدروکسید رسوب می کنند و بنابراین باعث خطا در محاسبه جرم باریم سولفات و در نهایت درصد سولفور خواهند شد. اما همیت کاتیونها در محیط اسیدی در آب محلول بوده و از کاغذ صافی شما رد خواهند شد.
بله درست می فرمایید.
سلام اگر میزان سولفات رو با این روش بیشتر از میزان واقعی محلول استاندارد به دست بیاوریم مشکل از چی میتونه باشه؟
منشا خطا رو باید پیدا کنید… معمولا چون این روش به کدورت وابسته س و کدورت ناشی از باریم سولفات هم زود تغییر میکنه باید خیلی روی زمان بندی تون دقت کنید.