روشهای اندازهگیری یون کلراید در آب
روشهای اندازهگیری یون کلراید در آب
یون کلراید
یون کلراید یکی از رایجترین آنیونهای موجود در منابع آبی است که در ترکیب با انواع کاتیونها مانند سدیم، منیزیم و کلسیم انواع مختلفی از نمکها را تولید میکند. طعم شوری ناشی از وجود یون کلراید، متفاوت و وابسته به آنالیز شیمیایی آب است. به عنوان نمونه، چنانچه کاتیون همراه آنیون کلراید، سدیم باشد طعم شوری در آب حاوی 250 mg/L احساس میشود. در حالیکه اگر کاتیون همراه، کلسیم یا منیزیم باشد، حتی در غلظتهای بیش از 1000 mg/L نیز طعم شوری احساس نخواهد شد. آب دریا و نفوذ آن به کرانههای ساحل، سنگهای نمکی، پسابهای صنعتی، خانگی، کشاورزی و کودهای شیمیایی از عوامل اصلی انتشار یون کلراید در آبهای سطحی و یا زیرزمینی محسوب میشوند.
یون کلراید در منابع آبی باعث افزایش هدایت الکتریکی آب شده و به همین جهت احتمال خوردگی در لولهها را افزایش میدهد. از طرفی، ممکن است واکنش یون کلراید با یونهای فلزی موجود در لولهها، باعث بالا بردن مقادیر فلزات در آب آشامیدنی شود. افزون بر این، غلظت بالای این یون، با اثرگذاری بر اکوسیستم موجودات آبزی، حیات آنها را به خطر میاندازد.
روشهای اندازهگیری یون کلراید
شش روش تیتراسیون رسوبی، پتانسیومتری، جیوه نیترات[1]، فریسیانید[2]، آنالیز تزریق جریان و الکتروفورز[3] برای تعیین آنیون کلراید وجود دارد. تیتراسیون رسوبی برای اندازهگیری مقادیر در حدود mg (0/15 تا 10) یون کلراید مناسب است. تکنیک پتانسیومتری برای نمونههای رنگی و یا کدر که تعیین نقطه پایان در آنها دشوار است، توصیه میشود. تعیین نقطه پایانی در روش جیوه نیترات بسیار راحت است. سه روش دیگر شامل روش فریسیانید، آنالیز تزریق جریان و الکتروفورز از جمله آنالیزهای دستگاهی به شمار میروند. هر چند استفاده از روشهای جیوه نیترات و تزریق جریان به دلیل سمیت بالای جیوه از نظر کاربردی و زیستمحیطی با محدودیتهای جدی مواجه هستند. از بین روشهای بیان شده، تنها به توضیح دو روش تیتراسیون رسوبی و پتانسیومتری پرداخته میشود.
1- تیتراسیون رسوبی
تیتراسیونها بر مبنای استفاده از نقره نیترات با نام «تیتراسیونهای نقرهسنجی[4]» شناخته شده و در تعیین یون کلرید شامل سه روش مور[5]، ولهارد[6] و فاجانز[7] میباشد.
الف- روش مور
این روش یکی از قدیمیترین انواع تیتراسیونهای رسوبی است که در سال 1865 توسط کارل فردریچ مور معرفی شد. در این تیتراسیون، از نقره نیترات و پتاسیم کرومات به ترتیب به عنوان تیترانت و شناساگر استفاده میشود. در ابتدا، با افزودن شناساگر به نمونه، رنگ محلول زرد خواهد شد. با انجام تیتراسیون، قبل از نقطه همارزی، به دلیل وجود یون کلراید در نمونه، افزودن پیوسته و قطره قطره نقره نیترات موجب تشکیل رسوب نقره کلراید سفید رنگ میشود. پس از نقطه همارزی و پایان یافتن یون کلراید، واکنش بین مقادیر اضافی نقره نیترات و یونهای کرومات منجر به ایجاد رنگ قرمز آجری خواهد شد.
واکنشهای شیمیایی به ترتیب، قبل و بعد از نقطه همارزی در این تیتراسیون به صورت زیر است:

مقدار کلراید بر حسب ppm را میتوان طبق رابطه زیر به دست آورد:

اگر آب مقطر به عنوان شاهد استفاده میشود، حجم مصرف شده تیترانت برای شاهد (Vtitrant for blank) و نمونه مجهول (Vtitrant) را ثبت نمایید. حجم بهدست آمده برای شاهد را از حجم بهدست آمده برای نمونه کم نموده (Vtitrant -Vtitrant for blank) و در محاسبات قرار دهید.
نکته مهم در روش مور، تنظیم pH محلول است. در این روش، pH محیط باید بین 7 تا 10 باشد. زیرا در محیطهای اسیدی، یونهای کرومات شناساگر، طی واکنش زیر، به دیکرومات تبدیل میشود:

از طرف دیگر، در محیطهای بازی نیز یونهای نقره به عنوان تیترانت با یونهای هیدروکسید موجود در محیط واکنش داده و در نهایت اکسید نقره تولید میکند که منجر به ایجاد خطا در تیتراسیون خواهد شد:
![]()
تداخلها: وجود یونهای برماید، یداید، سیانید، سولفید، سولفیت، تیوسولفات و اتیلن دیآمین تترااستیک اسید میتوانند در اندازهگیری یون کلراید در این روش، تداخل ایجاد کند. اورتوفسفات با غلظت بیش از 25 mg/L مزاحمت ایجاد میکند. وجود یونهای آهن با غلظت بالای 10 mg/L باعث عدم تشخیص نقطه پایان میشود.
تعیین یون کلراید با مزاحمت سولفیت
چنانچه غلظت یون سولفیت بیش از 10 ppm باشد، اندازهگیری یون کلراید با استفاده از روش مور با خطا مواجه خواهد بود. زیرا درحضور این یون، کلرین موجود در آب تبدیل به یون کلراید شده و باعث مصرف تیترانت و خطای مثبت میشود:
![]()
یکی از مهمترین روشها برای حذف این مزاحمت، بهرهگیری از یک اکسیدکننده قوی مانند هیدروژن پراکسید است. سولفیت موجود در نمونه با افزودن هیدروژن پراکسید، طی یک واکنش اکسایش – کاهش، به یون سولفات تبدیل شده و مزاحمت آن رفع میشود:
![]()
تعیین یون کلراید با مزاحمت EDTA
تعیین غلظت یون کلراید با استفاده از روش مور، در حضور EDTA با غلظت بیش از 50 ppm با خطای زیادی همراه است. تمایل زیاد EDTA به تشکیل پیوند با انواع یونهای فلزی و تشکیل کمپلکس، منجر به مصرف یونهای نقره شده و در تیتراسیون خطا ایجاد میکند:
![]()
جهت رفع این مزاحمت، از هیدروژن پراکسید و حرارت، استفاده میشود.
ب- روش ولهارد
در این روش از تکنیک تیتراسیون برگشتی جهت تعیین غلظت یون کلراید در نمونه آبی استفاده میشود. در مرحله اول، مقادیر مشخص و اضافی از نقره نیترات به محلول حاوی یون کلراید اضافه شده و رسوب سفید رنگ نقره کلراید تشکیل خواهد شد. چون مقادیر نقره نیترات افزوده شده، اضافی است، بنابراین همه محتوای یون کلراید موجود در محلول مصرف شده و به رسوب تبدیل میشود. محلول حاصل بعد از صاف شدن، با استفاده از پتاسیم تیوسیانات (KSCN) و در حضور شناساگر آهن (III) آمونیوم سولفات (FeNH4(SO4)2) تیتر میشود. تا قبل از نقطه همارزی، یونهای نقره با یونهای تیوسیانات واکنش داده و رسوب نقره تیوسیانات را تشکیل میدهد. در این حالت رنگ محلول حاصل زرد کمرنگ است:
![]()
در نقطه همارزی پس از اینکه همه نقره موجود در محلول مصرف شد، یون تیوسیانات موجود در محیط با یونهای آهن (III) شناساگر واکنش داده و کمپلکسی پایدار با رنگ قرمز تیره ایجاد خواهد شد که نشانگر نقطه پایانی و اتمام تیتراسیون است:
![]()
تداخلها: اندازهگیری غیرمستقیم یونهای هالید مهمترین ویژگی روش ولهارد است. در این روش، محیط اسید قوی مورد نیاز است که از مهمترین مزایای آن نسبت به سایر روشهای تیترسنجی برای اندازهگیری یونهای هالید است، زیرا یونهایی مانند کربنات، اکسالات و آرسنات (که موجب تشکیل نمکهای کم محلول در محیط خنثی میگردند) باعث تداخل نمیشود. اگر نمونه صاف نشود، واکنش زیر به دلیل اینکه انحلالپذیری رسوب نقره تیوسیانات کمتر از نقره کلراید است، رخ میدهد:
در نتیجه، مقادیر بیشتری از یون تیوسانات مصرف خواهد شد و اندازهگیری یون کلراید با خطای منفی همراه خواهد بود. این مشکل از طریق صاف کردن نقره کلراید قبل از تیتراسیون برگشتی برطرف میشود.
ج- روش فاجانز
تفاوت اصلی روش فاجانز با دو روش دیگر نقرهسنجی، استفاده از یک شناساگر جذب سطحی جهت تعیین نقطه پایانی تیتراسیون رسوبی است. شناساگر مورد استفاده در این تیتراسیون، معرف فلورسین[8] است که یک اسید ضعیف آلی است. شکل 1 ساختار شیمیایی فلورسین را نشان میدهد. وقتی فلورسین به محلول افزوده میشود کمی تفکیک شده و به یون هیدروژن و آنیون فلورسینات با رنگ زرد مایل به سبز تبدیل میشود.

شکل 1- ساختار مولکولی فلورسین
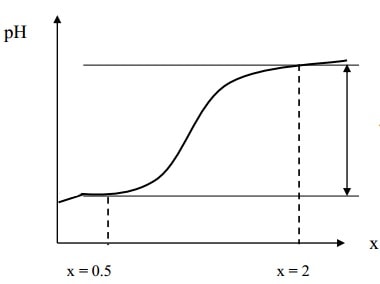
اساس عملکرد روش فاجانز بر مبنای تمایل کلوییدهای نقره کلراید به جذب سطحی یا واجذب شناساگر در محلول است. قبل از نقطه همارزی، یونهای منفی کلراید اضافی در محیط وجود دارند، بنابراین به صورت لایه اولیه بر سطح نقره کلراید جذب میشوند. در این حالت، بار سطحی این کلوییدها منفی شده و آنیون فلورسینات را از خود میرانند. بنابراین، این آنیون رنگ زرد مایل به سبز خود را نشان میدهد. اما پس از نقطه همارزی، یونهای مثبت نقره در محیط به صورت اضافی وجود دارند که بر سطح کلویید نقره کلراید جذب شده و به دلیل ایجاد بار سطحی مثبت، آنیون فلورسینات را جذب سطحی نموده و رسوب قرمز ایجد میکنند. این تغییر رنگ، نشانگر نقطه پایان تیتراسیون خواهد بود (شکل 2). به طور کلی pH مناسب برای انجام تیتراسیون بین 5 تا 8 میباشد.

شکل 2- روند تغییر بار سطحی کلوئید نقره کلرایدقبل و بعد از نقطه همارزی
تداخلها: در محلولهای بسیار اسیدی، یونهای مثبت هیدروژن با شناساگر دارای بار منفی واکنش میدهند. بنابراین غلظت شناساگر آزاد کاهش مییابد که منجر به ایجاد خطا در اندازهگیری خواهد شد. در محلولهای قلیایی نیز یونهای نقره بهجای تشکیل کلویید نقره کلراید، رسوب نقره هیدروکسید تشکیل میدهند و اندازهگیری غیرممکن میشود.
2- تیتراسیون پتانسیومتری
در این تیتراسیون، یون کلراید در اثر واکنش با محلول نقره نیترات تعیین میشود. ساختار کلی پیل الکتروشیمیایی به صورت زیر خواهد بود:
![]()
وظیفه الکترود مرجع در این تیتراسیون، ایجاد یک پتانسیل ثابت و پایدار در سیستم میباشد تا اینکه تغییرات پتانسیل الکترود نسبت به آن سنجیده شود. پتانسیل پیل (Ecell) مورد استفاده در اندازهگیری یون کلراید به صورت زیر است:

که در آن Eicd.، پتانسیل نیمپیل الکترود شناساگر و وابسته به غلظت گونههای موجود در محلول است و Eref. پتانسیل نیمپیل الکترود مرجع است که در طول تیتراسیون همواره ثابت است. در نیمپیل الکترود شناساگر، یونهای نقره تمایل دارند تا در واکنش کاهش شرکت نموده و به فلز نقره تبدیل شوند:

از آنجا که پتانسیل پیل تنها به غلظت یون نقره وابسته است، نمودار تغییرات پتانسیل پیل بر حسب مقدار یون افزوده شده رسم میشود. تغییر ناگهانی در منحنی تیتراسیون و یا وجود پیک در منحنی مشتق اول نشانگر پایان تیتراسیون خواهد بود.
[1] Mercuric nitrate method
[2] Automated ferricyanide method
[3] electrophoresis
[4] Argentometric method
[5] Mohr method
[6] Volhard mothod
[7] Fajans method
[8] fluorescein
منبع:
اسد آبادی، سمین و همکاران، (1399)، کنترل کیفیت آب مبانی و روشها، انتشارات دانشگاه بوعلی سینا